Макромир
2.3.2. Макромир
От микромира к макромиру. Теория строения атома дала химии ключ к познанию сущности химических реакций и механизма образований химических соединений – более сложного молекулярного уровня организации вещественной материи по сравнению с элементной атомной формой.
Квантовая механика позволила решить очень важный вопрос о расположении электронов в атоме и установить зависимость свойств элементов от строения электронных оболочек. В настоящее время разработаны схемы строения атомов всех химических элементов. При их построении ученые исходили из общих соображений об устойчивости различных комбинаций электронов. И естественно, что путеводной нитью при этом служил периодический закон Д.И. Менделеева.
При разработке схем строения атомов элементов учитывалось следующее:
-
принималось, что число электронов в атоме равно заряду атомного ядра, т.е. порядковому номеру элемента в периодической системе;
-
вся электронная оболочка распадается на несколько слоев соответствующих определенным энергетическим уровням (n = 1, 2,3,4,…);
-
на каждом уровне п может находиться не более N электронов, где N= 2п2;
-
состояние каждого электрона в атоме определяется совокупностью четырех квантовых чисел п, l, т и s.
В соответствии с принципом Паули все электроны в атоме отличаются друг от друга хотя бы одним квантовым числом. В атоме нет двух электронов, у которых все квантовые числа одинаковы, соответствии с указанными допущениями построены упрощенные схемы строения атомов для первых трех периодов таблицы Менделеева.
Несмотря на условность и простоту этих схем, они тем не менее достаточны для объяснения важнейших свойств элементов и ия соединений.
Так, например, на первом энергетическом уровне ( n = 1,
l =0, т = 0) могут находиться только два электрона, отличающиеся своими спиновыми квантовыми числами (s = ±1/2). Других электронов при п = 1 быть не может. Это соответствует тому, что если на первом уровне имеется один электрон, то это — атом водорода; если два электрона, то это – атом гелия. Оба элемента заполняют первый ряд таблицы Менделеева.
Второй ряд таблицы Менделеева занимают элементы, электроны которых расположены на втором энергетическом уровне (п = 2). Всего на втором энергетическом уровне может быть восемь электронов (N=2·22).
Действительно, при п = 2 могут иметь место следующие состояния электронов: если l = 0 и т
= 0, то может быть два электрона с противоположными спинами; если l = 1, то т
может принимать три значения (т = –1; 0; +1), и каждому значению т
соответствует также по два электрона с разными спинами. Таким образом, всего будет восемь электронов.
Второй ряд элементов в таблице Менделеева, у которых последовательно добавляется по одному электрону на втором энергетическом уровне, — литий, бериллий, бор, углерод, азот, кислород, фтор, неон.
При главном квантовом числе п = 3 l может принимать три значения (l =0; 1; 2), а каждому l соответствует несколько значений т. при l = 0 т
= 0; при l ~ 1 т
= –1; 0; +1; при l=2 т
= –2; -1; 0; I 1; +2 (рис. 2.4).
Так как всего может быть девять значений т, а каждому состоянию т
соответствует два электрона с разными значениями s = ±1/2, nо всего на третьем энергетическом уровне (п = 3) может быть 18 электронов (N = 2·З2).
Третий ряд в таблице Менделеева соответствует последовательному заполнению электронами внешнего энергетического уровня у элементов от натрия до аргона (натрий, магний, алюминий, кремний, фосфор, сера, хлор, аргон).
Энергетические уровни и возможные состояния электронов в атоме:
возможные орбиты, на которых электрон в атоме движется вокруг ядра, можно изобразить в виде окружностей (А), в каждой из которых точно укладывается целое число длин световых волн, равное главному квантовому числу п. Двумерный аналог атома может быть описан двумя квантовыми числами, а реальный атом характеризуют три квантовых числа.
Следующие ряды периодической системы соответствуют более сложным правилам заполнения внешних уровней атомов электронами, поскольку при увеличении общего числа электронов, а атомах начинают проявляться коллективные взаимодействия между разными группами электронов, расположенных на разных энергетических уровнях. Это приводит к необходимости учитывать ряд более тонких эффектов.
Выяснение строения электронных оболочек атомов оказало влияние и на саму структуру периодической системы, несколько изменив существовавшее до тех пор деление элементов на периоды. В прежних таблицах каждый период начинался с инертного газа, причем водород оставался вне периодов. Но теперь стало ясно, что новый период должен начинаться с того элемента, в атоме которого впервые появляется новый электронный слой в виде одного валентного электрона (водород и щелочные металлы), и заканчиваться тем элементом, в атоме которого этот слой имеет восемь электронов, образующих очень прочную электронную структуру, свойственную инертным газам.
Теория строения атомов разрешила также вопрос о положении в периодической системе редкоземельных элементов, которые ввиду их большого сходства друг с другом нельзя было распределить по различным группам. Атомы этих элементов отличаются друг от друга строением одного из внутренних электронных слоев, в то время как число электронов в наружном слое, от которого главным образом зависят химические свойства элемента, у них одинаково. По этой причине все редкоземельные элементы (лантаноиды) помещены теперь вне общей таблицы.
Однако основное значение теории строения атомов заключалось в раскрытии физического смысла периодического закона, который, но времена Менделеева был еще неясен. Достаточно взглянуть на таблицу расположения электронов в атомах химических элементов, чтобы убедиться, что с увеличением зарядов атомных ядер постоянно повторяются одни и те же комбинации электронов в наружном слое атома. Таким образом, периодическое изменение свойств химических элементов происходит вследствие периодического возвращения к одним и тем же электронным конфигурациям.
Попытаемся установить более точно, в какой зависимости от строения электронных оболочек находятся химические свойства атомов.
Рассмотрим сначала изменение свойств в периодах. В пределах каждого периода (кроме первого) металлические свойства, наиболее резко выраженные у первого члена периода, при переходе к последующим членам постепенно ослабевают и уступают место металлоидным свойствам: в начале периода стоит типичный металл, в конце – типичный металлоид (неметалл) и за ним – инертный газ.
Закономерное изменение свойств элементов в периодах может быть объяснено следующим образом. Наиболее характерным свойством металлов с химической точки зрения является способность их атомов легко отдавать внешние электроны и превращаться в положительно заряженные ионы, тогда как металлоиды, наоборот, характеризуются способностью присоединять электроны с образованием отрицательных ионов.
Для отрыва электрона от атома с превращением последнего в положительный ион нужно затратить некоторую энергию, которая называется потенциалом ионизации.
Потенциал ионизации имеет наименьшее значение у элементов, начинающих период, т.е. у водорода и щелочных металлов, и наибольшее – у элементов, заканчивающих период, т.е. у инертных газов. Величина его может служить мерой большей или меньшей «металличности» элемента: чем меньше потенциал ионизации, чем легче оторвать электрон от атома, тем сильнее должны быть выражены металлические свойства элемента.
Величина потенциала ионизации зависит от трех причин:
от величины заряда ядра, радиуса атома и особого рода взаимодействия между электронами в электрическом поле ядра, вызванного их волновыми свойствами. Очевидно, что чем больше заряд ядра и чем меньше радиус атома, тем сильнее притягивается электрон к ядру тем больше потенциал ионизации.
У элементов одного и того же периода при переходе от щелочного металла к инертному газу заряд ядра постепенно возрастает, а радиус атома уменьшается. Следствием этого и является постепенное увеличение потенциала ионизации и ослабление металлических свойств. У инертных газов, хотя радиусы их атомов больше, чем радиусы атомов галогенов, стоящих в том же периоде, потенциалы ионизации больше, чем у галогенов. В этом случае сильно сказывается действие третьего из вышеупомянутых факторов – взаимодействия между электронами, вследствие чего внешняя электронная оболочка атома инертного газа имеет особую энергетическую устойчивость, и удаление из нее электрона требует значительно большей затраты энергии.
Присоединение электрона к атому металлоида, превращающее его электронную оболочку в устойчивую оболочку атома инертного газа, сопровождается выделением энергии. Величина этой энергии при расчете на 1 грамм-атом элемента служит мерой так называемого сродства к электрону. Чем больше сродство к электрону, тем легче атом присоединяет электрон. Сродство атомов металлов к электрону равно нулю, – атомы металлов не способны присоединять электроны. У атомов же металлоидов сродство к электрону тем больше, чем ближе к инертному газу стоит металлоид в периодической системе. Поэтому в пределах периода металлоидные свойства усиливаются по мере приближения к концу периода.
В повседневной жизни нам не приходится иметь дело с атомами. Окружающий нас мир построен из объектов, образованных из гигантского числа атомов в виде твердых тел, жидкостей и газов. Следовательно, нашим следующим шагом должно быть изучение того, как атомы взаимодействуют друг с другом, образуя молекулы, а затем и макроскопическое вещество. Даже человеческая индивидуальность (и вообще поведение всех живых организмов) является результатом различий в структурах гигантских молекул, несущих генетическую информацию.
Молекулы состоят из одинаковых или различных атомов, соединенных между собой межатомными химическими связями. Устойчивость молекул свидетельствует о том, что химические связи обусловлены силами взаимодействия, связывающими атомы в молекулу.
Силы межатомного взаимодействия возникают между внешними электронами атомов. Потенциалы ионизации этих электронов значительно меньше, чем у электронов, находящихся на внутренних энергетических уровнях.
Нахождение конкретных формул химических соединений значительно упрощается, если воспользоваться понятием о валентности элементов, т.е. свойством его атомов присоединять к себе или замещать определенное число атомов другого элемента.
Понятие о валентности распространяется не только на отдельные атомы, но и на целые группы атомов, входящие в состав химических соединений и участвующие как одно целое в химических реакциях. Такие группы атомов получили название радикалов.
Физические основы химических связей в молекулах вещества. Однако природа сил, обусловливающих связь между атомами в молекулах, долгое время оставалась неизвестной. Только с развитием учения о строении атома появились теории, объясняющие причину различной валентности элементов и механизм образования химических соединений на основе электронных представлений. Все эти теории основываются на существовании связи между химическими и электрическими явлениями.
Остановимся, прежде всего, на отношении веществ к электрическому току.
Одни вещества являются проводниками электрического тока, как и твердом, так и в жидком состоянии: таковы, например, все металлы. Другие вещества в твердом состоянии тока не проводят, но элекропроводны в расплавленном виде. К ним принадлежит огромное большинство солей, а также многие окислы и гидраты окислов. Наконец, третью группу составляют вещества, не проводящие тока ни в твердом, ни в жидком состоянии. Сюда относятся почти все металлоиды.
Опытом установлено, что электропроводность металлов обусловлена движением электронов, а электропроводность расплавленных солей и им подобных соединений – движением ионов, имеющих противоположные заряды. Например, при прохождении тока через расплавленную поваренную соль к катоду движутся положительно заряженные ионы натрия Na+, а к аноду – отрицательно заряженные ионы хлора Сl–. Очевидно, что в солях ионы существуют уже в твердом веществе, расплавление лишь создаст условия для их свободного движения. Поэтому такие соединения получили название ионных соединений. Вещества, практически не проводящие тока, не содержат ионов: они построены из электрически нейтральных молекул или атомов. Таким образом, различное отношение веществ к электрическому току является следствием различного электрического состояния частиц, образующих эти вещества.
Указанным выше типам веществ отвечают два различных типа химической связи:
а)ионная связь, иначе называемая электровалентной (между противоположно заряженными ионами в ионных соединениях);
б)атомная, или ковалентная, связь (между электронейтральными атомами в молекулах всех остальных веществ).
Ионная связь.
Такого типа связь существует между противоположно заряженными ионами и образуется в результате простого электростатического притяжения ионов друг к другу.
Положительные ионы образуются путем отщепления от атомов электронов, отрицательные – путем присоединения электронов к атомам.
Так, например, положительный ион Na+ образуется при отщеплении от атома натрия одного электрона. Так как в наружном слое атома натрия находится только один электрон, то естественно предположить, что именно этот электрон, как наиболее удаленный от ядра, и отщепляется от атома натрия при превращении его в ион. Подобным же образом ионы магния Mg2+ и алюминия А13+ получаются в результате отщепления от атомов магния и алюминия соответственно двух и трех внешних электронов.
Напротив, отрицательные ионы серы и хлора образуются путем присоединения к этим атомам электронов. Поскольку внутренние электронные слои в атомах хлора и серы заполнены, дополнительные электроны в ионах S2 и Сl–, очевидно, должны были занять места во внешнем слое.
Сравнивая состав и строение электронных оболочек ионов Na+, Mg2+, А13+, мы видим, что у всех этих ионов они одинаковы – такие же, как у атомов инертного газа неона (Ne).
В то же время ионы S2 и Сl–, образующиеся в результате присоединения электронов к атомам серы и хлора, имеют такие же электронные оболочки, как и атомы аргона (Аг).
Таким образом, в рассмотренных случаях при превращении атомов в ионы электронные оболочки ионов уподобляются оболочкам атомов инертных газов, наиболее близко к ним расположенных в периодической системе.
Современная теория химической связи объясняет это тем, что электронные группировки в атомах инертных газов (два электрона в наружном слое атома гелия и восемь электронов в атомах остальных инертных газов) являются особенно устойчивыми. Именно вследствие устойчивости этих группировок инертные газы и не способны вступать в соединение с другими элементами. Атомы, имеющие в наружном слое менее восьми электронов, стремятся приобрести структуру инертных газов, отдавая «лишние» электроны или пополняя их число в своем наружном слое до восьми за счет электронов других атомов, что и происходит при образовании большинства химических соединений, состоящих из ионов.
Процесс образования химического соединения ионного типа из атомов можно представить следующим образом.
Сначала атомы превращаются в разноименно заряженные ионы вследствие перехода электронов от одного атома к другому, а затем уже ионы взаимно притягиваются, образуя соединение с ионной связью.
Положим, например, что
атомы натрия, имеющие в наружной оболочке только один электрон, встречаются с атомами хлора, наружная оболочка которых содержит семь электронов. Атомы натрия отдают свои «лишние» электроны, атомам хлора, превращаясь в положительные однозарядные ионы с электронной конфигурацией инертного газа неона. В то же время атомы хлора, присоединившие к своему наружному слою по одному электрону, становятся отрицательными однозарядными ионами со структурой атомов аргона. После этого сила электрического притяжения между разноименными зарядами связывает образовавшиеся ионы друг с другом, в результате чего получается соль – хлористый натрий (рис. 3).
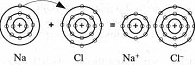
Рис.3. Схема образования хлористого натрия
Изложенные выше представления о механизме образования ионных соединений приводят к заключению, что валентность элементов в ионных соединениях характеризуется числом электрических зарядов их ионов. Иначе ее называют электровалентностью.
Величина электровалентности определяется числом электронов, отданных атомом при образовании положительного иона или присоединившихся к нему при образовании отрицательного иона. В первом случае электровалентность считается положительной, во втором – отрицательной.
Способность атомов превращаться в положительные или отрицательные ионы зависит от положения соответствующих элементов в периодической системе. Атомы элементов, стоящих в начале периода, имеют меньший заряд ядра, чем атомы элементов, находящиеся в конце периода. В первом случае электроны притягиваются слабее, чем во втором, поэтому склонность атомов к превращению в положительные ионы, вообще говоря, уменьшается в периоде в направлении слева направо.
Ковалентная связь. Предположение об электростатическом притяжении между противоположно заряженными ионами, как о причине возникновения химической связи, явно неприменимо к молекулам простых веществ (водорода Н2, кислорода О2 и др.), а также к молекулам веществ, образованных близкими по химическим свойствам элементами, так как в этом случае трудно допустить возникновение противоположно заряженных ионов. Поэтому по отношению к таким веществам бьиа выдвинута другая теория их образования, получившая название теории ковалентных связей. При разработке этой теории тоже учитывалась химическая устойчивость атомов инертных газов.
Согласно теории ковалентных связей при образовании молекул (как и при образовании ионных соединений) атомы химических элементов приобретают устойчивые электронные оболочки, подобные оболочкам атомов инертных газов. Однако устойчивость эта достигается не путем перехода электронов от одних атомов к другим, а путем образования одной или нескольких пар электронов, которые становятся общими для соединяющихся атомов, т.е. входят одновременно в состав электронных оболочек двух атомов. Можно представить себе, что эти «спаренные» электроны вращаются по орбитам, охватывающим ядра обоих атомов, и таким образом связывают атомы в молекулу.
Химическая связь, обусловленная наличием электронных пар, называется ковалентной, или атомной, связью, в отличие от электровалентной, или ионной, связи, основанной на электростатическом притяжении между разноименно заряженными ионами.
Предположение о паре электронов, как бы «обслуживающей» два ядра, как о причине возникновения ковалентной связи получило обоснование в волновой механике. Два положительно заряженных ядра можно рассматривать как одно ядро с большим зарядом, чем у каждого из ядер в отдельности. Электрон, вращающийся вокруг такого комбинированного ядра, удерживается более сильно, чем, если бы он вращался около одного из ядер. Этим объясняется энергетическая выгодность образования ковалентных связей. Новая орбит движения электрона в молекуле называется молекулярной. Движение электронов по молекулярным орбитам подчиняется тому же правил Паули, что и движение по атомным орбитам. Поэтому на одной той же молекулярной орбите не может быть больше двух электронов, причем они должны иметь противоположные спины. Электроны одинаковыми спинами на одной и той же молекулярной орбите находиться не могут. Вот почему каждая ковалентная связь образована лишь парой электронов.
Образование молекулярных орбит с точки зрения волновой механики является следствием «перекрывания» атомных орбит. В результате такого перекрывания наибольшая электронная плотность молекулярной орбите, если ее представить, как электронное облако оказывается между ядрами. Это значит, что электроны при движении по молекулярной орбите наиболее часто попадают в область, находящуюся между ядрами. В результате между ядрами создается как бы прослойка из отрицательного электричества, способствующая сближению ядер. Поэтому чем сильнее «перекрываются» атомные орбиты при образовании молекулярных орбит, тем прочнее связь. Валентность или, точнее, ковалентность элемента в данном соединена, определяется числом электронов его атома, идущих на образование общих, или «связующих», электронных пар.
Итак, ковалентная связь между атомами в молекулах обусловливается наличием одной или нескольких общих пар электронов. Так как при образовании ковалентной связи, как правило, не происходит ни потери, ни присоединения электронов к атомам, то понятно, что молекулы с ковалентной связью не содержат ионов. Примером молекул с ковалентной связью может служить вода (Н2,О).
Одним из элементов, образующих ковалентные связи, является углерод. Углерод участвует в молекулярных структурах почти всегда с четырьмя ковалентными связями.
Большая часть животного и растительного мира образована соединениями углерода (С) с водородом (Н) и некоторыми другими элементами, прежде всего азотом (N), кислородом (О), фосфором (Р) и серой (S). Эти соединения первоначально называли органическими соединениями, в отличие от ионных (неорганических), так как по своему химическому составу все животные и растения почти на 98% состоят из указанных шести химических элементов.
Простейшими из органических молекул являются углеводороды, состоящие только из атомов углерода и водорода. Каждая черточка – ковалентная связь, осуществляемая двумя электронами. При комнатной температуре первые четыре вещества данного углеводородного ряда – газы, следующие десять –жидкости, а все последующие – твердые вещества, или парафины.
Сложные органические соединения содержат ряд других элементов. Так, все органические кислоты (например, лимонная) и все спирты (например, этиловый) содержат кислород.
Многие молекулы в живой природе, в частности молекулы белков, чрезвычайно сложны. Несмотря на это, в последнее время были достигнуты большие успехи в определении состава, структуры и функции этих молекул. В частности, многое стало известно о структуре ДНК (дезоксирибонуклеиновой кислоты), несущей генетическую информацию. Хотя эта молекула может содержать до миллиона атомов, ДНК точно воспроизводится при делении клеток, что обеспечивает в ряду поколений клеток и организмов передачу наследственных признаков и специфических форм обмена веществ.
После того, как была выяснена природа сил, приводящих к объединению атомов в молекулы, т.е. природа «химизма», проявляющаяся в огромном многообразии химических превращений вещества, в том числе приводящая к образованию многоатомных сложных молекул, стал ясен механизм первой ступени самоорганизации материи в природе от более простых атомных систем к гораздо более сложным молекулярным системам. Диапазон известных молекулярных структур огромен – от двухатомных молекул типа Н2, О2 до макромолекул органических соединений, состоящих из сотен и тысяч атомов, – белков и нуклеиновых кислот.
Из огромной совокупности разных молекул состоит все неживое и живое вещество природы – макротела. Количественные изменения при переходе от микрообъектов (атомов, молекул) к макротелам большой совокупности микросистем – приводят к существенным качественным изменениям в поведении, следовательно, в описании этих объектов исследования.
На макроуровне принято отдельно рассматривать вещественную молевую материю. Вещество может находиться в четырех агрегатных состояниях – твердые тела, жидкости, газы, плазма. Все явления и процессы в макромире связаны с процессами сохранения и преобразования одних форм движения в другие на основе двух всеобъемлющих законов – закона сохранения и превращения энергии и закона возрастания энтропии.
Указанные макропроцессы изучаются в рамках так называемой физической картины мира – в виде законов механики, статистической фишки, термодинамики и электродинамики. А вся совокупность явлений макромира изучается многочисленными естественно-научными дисциплинами (физикой, химией, геологией, биологией и т.д.).

Оставьте комментарий!
Вы должны быть авторизированы чтобы оставлять комментарии.